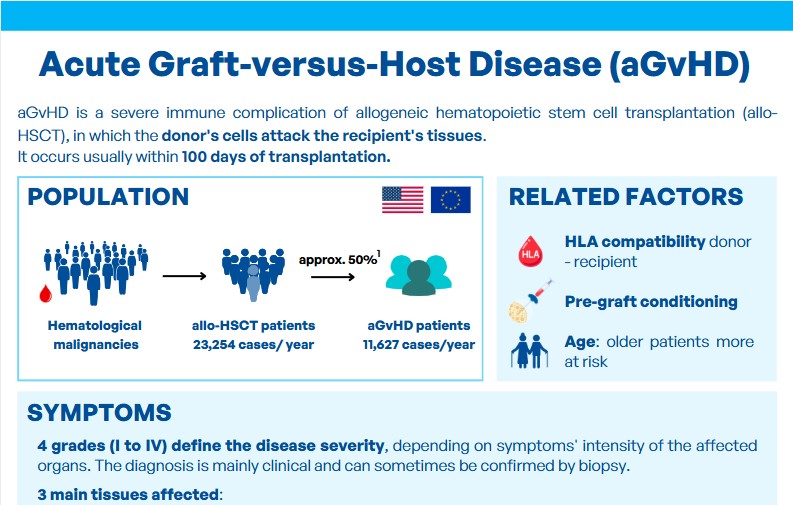
La maladie du greffon contre l’hôte ou la GvH (Graft-versus-Host Disease) est l’une des potentielles complications après une greffe allogénique de cellules souches hématopoïétiques (CSH). On estime 30 à 50% des patients qui déclarent une GvH après une greffe allogénique de CSH.
Professionnels de santé
Cette page s'adresse aux professionnels de santé.
GvH : pathologie et épidémiologie
On distingue deux types de GvH qui se caractérisent, entre autres, par le temps d’apparition des symptômes : 100 jours après la greffe, on parle de GvH aiguë et au-delà, on parle de chronique. Les symptômes diffèrent également entre ces deux formes.
- La GvH chronique est plus diffuse dans l’apparition des symptômes. En effet, elle touche aussi bien la peau, les yeux, la bouche, les muscles, le tractus gastro-intestinal, et peut engendrer des infections et des difficultés à respirer.
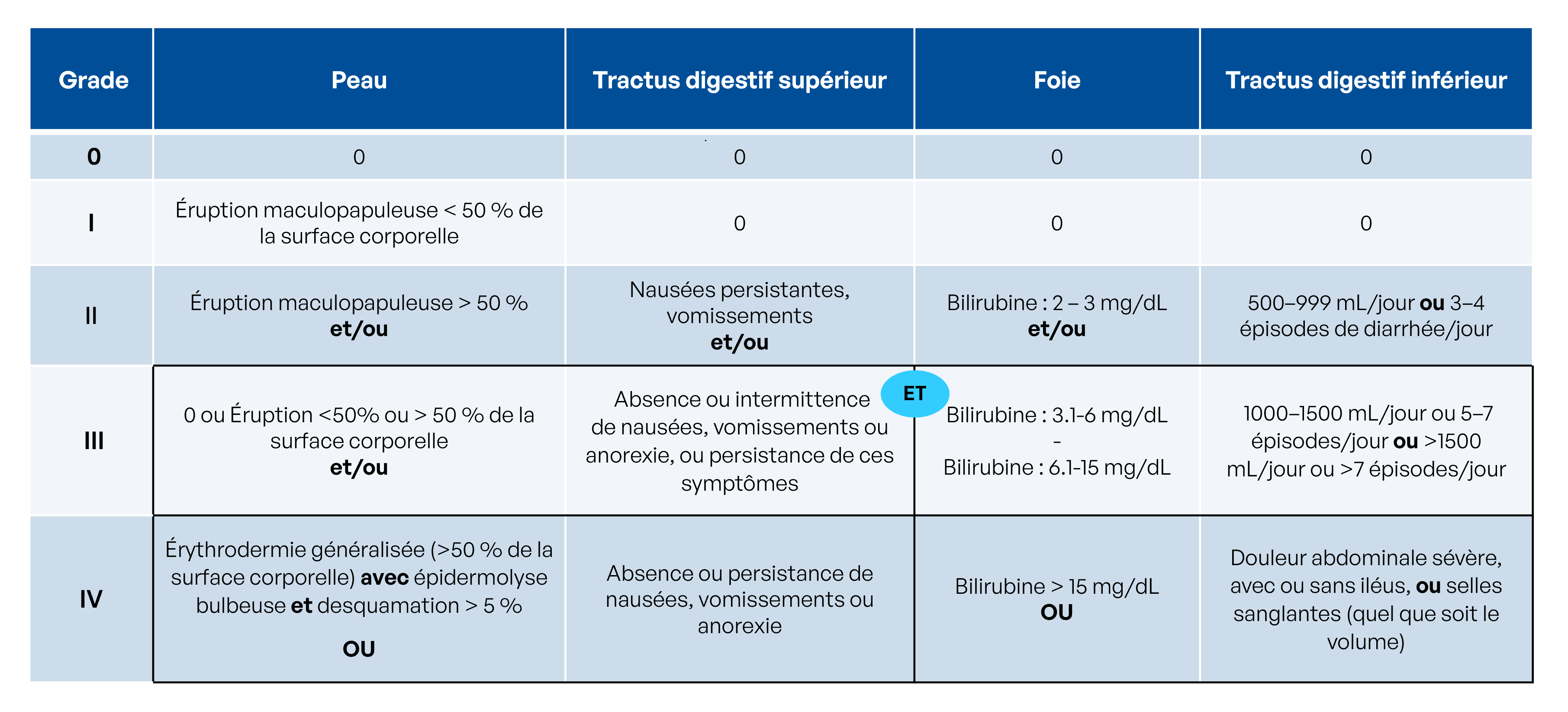
- La GvH aiguë est, quant à elle, plus localisée sur 3 organes : la peau, le foie et le tractus gastro-intestinal. La GvH aiguë peut être fulgurante et engendrer le décès du patient rapidement. C’est une des complications les plus redoutées après une allogreffe de CSH et elle est généralement de moins bon pronostic.
Lors d’une allogreffe de CSH, malgré la rigoureuse sélection du donneur sur la base du système HLA, il est possible que le greffon attaque les tissus du patient, qu’il considère comme étrangers.
Le microbiote intestinal : une voie innovante dans la prise en charge des cancers du sang
Dans les hémopathies malignes, le microbiote intestinal émerge comme un acteur clé dans la modulation de la réponse immunitaire et l’efficacité des traitements. La dysbiose induite par la maladie elle-même, les chimiothérapies ou les antibiotiques pourrait contribuer à une inflammation systémique. Des études récentes montrent que la restauration du microbiote, pourrait améliorer la tolérance aux traitements, réduire le risque de complications comme la GVH post-allogreffe, et potentiellement prolonger la survie des patients. Ces avancées ouvrent de nouvelles perspectives thérapeutiques en hémato-oncologie.
En savoir plus 👇
- Malard et.al, 2022 – Faecal microbiota transplantation in patients with haematological malignancies undergoing cellular therapies: from translational research to routine clinical practice (The Lancet Haematology)
- Chang, C. C., Hayase, E., & Jenq, R. R. 2021. The role of microbiota in allogeneic hematopoietic stem cell transplantation (Expert Opinion on Biological Therapy)
- Peled et al., 2020 — Microbiota as predictor of mortality in allogeneic hematopoietic-cell transplantation (New England Journal of Medicine)
- Galloway-Peña et al., 2019 — “Fecal Microbiome, Metabolites, and Stem Cell Transplant Outcomes: A Single-Center Pilot Study” (Open Forum Infectious Diseases)
- Kakihana et al., 2016 — “Fecal microbiota transplantation for patients with steroid-resistant acute graft-versus-host disease of the gut” (Blood)
- Shono et al., 2016 — Increased GVHD-related mortality with broad-spectrum antibiotic use after allogeneic hematopoietic stem cell transplantation in human patients and mice (Science Translational Medicine)
- Jenq et al., 2015 — “Intestinal Blautia Is Associated with Reduced Death from Graft-versus-Host Disease” (Biology of Blood and Marrow Transplantation)
Avis d’expert sur l’aGvH : impact sur le microbiote et approches thérapeutiques – Pr Florent Malard
Programme d’accès compassionnel
Les études cliniques sont cruciales pour démontrer la sécurité et l’efficacité des nouveaux traitements, permettant aux autorités réglementaires d’autoriser leur mise sur le marché. Toutefois, lorsqu’aucune alternative thérapeutique n’existe pour des patients aux besoins importants, des mécanismes locaux permettent un accès précoce aux médicaments avant leur autorisation officielle, sous conditions strictes et en accord avec les autorités compétentes. L’Autorisation d’Accès Compassionnel (AAC) octroyée par l’ANSM est une procédure permettant l’utilisation, à titre exceptionnel, d’un médicament dans une indication précise en l’absence de demande d’autorisation de mise sur le marché (AMM) ou avant la délivrance d’une telle AMM pour ce médicament.
Toutes les conditions suivantes sont à remplir pour réaliser une demande :
- Le médicament est destiné à traiter une maladie grave, rare ou invalidante,
- Il n’existe pas de traitement approprié,
- Le médicament ne fait pas l’objet d’une recherche impliquant la personne humaine (RIPH) à des fins commerciales,
- ou, lorsque le médicament fait l’objet d’une RIPH à des fins commerciales, le patient ne peut participer à cette recherche, la mise en œuvre du traitement ne peut pas être différée, et le laboratoire s’est engagé à déposer une demande d’accès précoce,
- L’efficacité et la sécurité du médicament sont présumées au regard des données cliniques disponibles.
MaaT Pharma collabore étroitement avec l’ANSM pour le suivi des patients bénéficiant d’un accès compassionnel selon les modalités fixées dans le Protocole d’Utilisation Thérapeutique et de Suivi des Patients (PUT-SP) le cas échéant. Le référentiel des accès compassionnels en cours est disponible sur le site de l’ANSM. Toute demande pour faire bénéficier un patient d’un accès compassionnel en cours se fait via le site de l’ANSM « e-Saturne ».
Pour toute question relative au programme d’accès compassionnel, vous pouvez nous contacter.
Essais cliniques, données cliniques et publications scientifiques
Essais Cliniques
- MaaT013 – Essai clinique de phase III – ARES: https://clinicaltrials.gov/study/NCT04769895
- MaaT033 – Essai clinique de phase II – PHOEBUS: https://clinicaltrials.gov/study/NCT05762211
Données Cliniques
Résultats Principaux Phase III Pivotale (MaaT013): ARES
Programme d’accès compassionnel
- Données présentées au congrès de l’ASH en décembre 2024 et au Congrès de l’EHA en juin 2025
- En savoir plus sur l’Accès dérogatoire en France – Lien vers le site internet de l’ANSM
Publications Scientifiques
Management de l’aGvH
- Abedin et al., 2021 – Ruxolitinib resistance or intolerance in steroid-refractory acute graft-versus-host disease – a real-world outcomes analysis (British Journal of Haematology)
- Penack O et al.,2021 – Prophylaxis and management of graft-versus-host disease after stem-cell transplantation for haematological malignancies: updated consensus recommendations of the European Society for Blood and Marrow Transplantation (The Lancet Haematology)
- , , , , , , et al.(2012) – First and second-line systemic treatment of acute graft-versus-host disease: recommendations of the American society of blood and marrow transplantation. (Biol Blood Marrow Transplant)
- Ferrara JL et al., 2009 – Graft-versus-host disease (The Lancet)
Microbiote intestinal & GvH
- Malard F et al. (2023) – Pooled allogeneic faecal microbiota MaaT013 for steroid-resistant gastrointestinal acute graft-versus-host disease: a single-arm, multicentre phase 2 trial. (eClinicalMedicine)
- Malard F. et al. (2021) – Restoration of gut microbiota diversity with autologous fecal microbiota transfer in acute myeloid leukemia patients. (Nature communications)
- Malard F. et al. (2018) – High gastrointestinal microbial diversity and clinical outcome in graft-versus-host disease patients (Bone Marrow Transplantation)
Production & Process
- Gefen, R., Dourado, J., Emile, S.H. et al.(2025) – Fecal microbiota transplantation for patients with ulcerative colitis: a systematic review and meta-analysis of randomized control trials. Techniques in Coloproctology – Springer Nature
- Reygner.et al. (2024) – Reduction of product composition variability using pooled microbiome ecosystem therapy and consequence in two infectious murine models (Applied and Environmental Microbiology – ASM Journals)
- Laperrousaz B. et al (2024) – Safety comparison of single-donor and pooled fecal microbiota transfer product preparation in ulcerative colitis: systematic review and meta-analysis. (BMC Gastroenterology)